Comme pour les saisons précédentes, je vais revenir sur la saison d’Orphan Black qui vient d’être diffusée. Mais pour une fois, je vais commencer par article concernant des éléments relevant du milieu de saison. Un autre sur des éléments présents plutôt dans la saison est en préparation. Un troisième arrivera peut-être mais son sujet n’étant pas défini, rien n’est sûr. Comme d’habitude, cet article contiendra des éléments important de l’intrigue, il est donc préférable de visionner la série avant lire l’article et de cliquer sur les zones du texte qui est masqué.
[spoiler]Après la mort du Dr Leekie, les clones se retrouvent à faire face à une branche de la Neolution avec BrightBorn Industries. Si le premier faisait de la biologie de synthèse en écrivant le génome des clones, les seconds modifient et éditent les génomes pour créer des bébés sans défauts. Comme le dit Evie Cho leur représentante le dit si bien :[/spoiler]
And as an engineer, when I see a flaw, I wanna fix it. (épisode 5)
En tant qu’ingénieure, quand je vois un défaut, je veux le réparer. (traduction personnelle)
Mais quand est-il dans la réalité ? Est-il si simple de modifier un gène ? Est-il possible changer l’évolution d’une espèce ? Une technologie récente semble en effet promettre ça. Il s’agit de la méthode CRISPR-Cas9.

Les bactéries vs les virus (bactériophages)
Bien que très diversifiées, les eubactéries et les archaebactéries doivent se défendre contre des virus qui veulent parasiter leurs systèmes de production de protéines, d’ADN et/ou d’ARN pour se dupliquer, comme tous les êtres vivants. Comme la plupart de ces virus injecte uniquement leur ADN (ou dans de rare cas leur ARN), les bactéries développent des mécanismes de défense basés sur la reconnaissance et la destruction de l’ADN viral (elles ont également d’autres méthodes mais nous les développerons pas ici). Une des solutions est de « marquer » l’ADN de la bactérie en ajoutant des groupements méthyl sur certaines séquences précises (et courte). Si un ADN présente ces séquences sans le méthyl alors il sera coupé en petits morceaux inoffensifs (ils ne pourront pas être traduits en protéines). D’autres ont, dans leur propre génome, des parasites de virus qui empêcheront l’assemblage de nouveaux virus à partir des éléments produit par la bactérie infectée à partir de l’ADN viral.
Le dernier mécanisme est celui qui nous intéresse à savoir le système CRISPR-Cas (proncé crispère). Certaines bactéries ont un système immunitaire qui garde une « mémoire » des virus qu’elles ont croisés. Elles sont en quelque sorte vaccinées. Dans leurs génomes, elles ont des CRISPR (clustered regularly interspaced short palindromic repeats), de courtes séquences dyadiques (comme DYAD institut) qui sont répétées et espacées par de courte séquence ADN provenant de virus. Avant ces séquences se trouvent des gènes codant pour des enzymes dites Cas pour CRISPR-associated. Certaines de ces enzymes vont servir à incorporer de nouvelles séquences d’ADN viral en cas d’infection viral tandis que d’autres vont utiliser une copie ARN des CRISPR et des séquences intercalées pour rechercher de l’ADN viral (qui se collera à l’ARN) et le détruire en le coupant en morceaux.
La méthode CRISPR-Cas9
En 2012, les chercheuses Emmanuelle Charpentier et Jennifer Doudna ont légèrement modifié ce mécanisme pour obtenir un outil pour éditer les génomes. Il s’agit d’utiliser l’enzyme CRISPR-Cas9 avec un ARN synthétisé. La synthèse de l’ARN permet de choisir précisément la cible dès que la séquence est connue et est très rapide à obtenir avec les techniques actuelles. De nouvelles modifications de CRISPR-Cas9 permettent d’empêcher un gène d’être utilisé ou au contraire de l’activer. Enfin il est possible de modifier la version d’un gène, par exemple lié à une maladie, CRISPR-Cas9 cible et coupe l’ADN au niveau de la zone à modifier du gène et de petits morceaux d’ADN sont introduits avec la version voulue du gène. La cellule cherchant toujours à recoller les morceaux d’ADN, elle utilisera les morceaux d’ADN comme guide pour réparer l’ADN et la version du gène voulue sera introduite dans le génome.
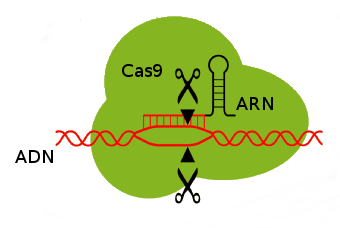
La méthode CRISP-Cas9 est plus précise, plus rapide et moins chères que les autres techniques d’édition génomique. Elle permet d’obtenir très rapidement des cellules ou des organismes modifiés et à faible coût. Elle a donc été rapidement adopter par les laboratoires de recherche qui peuvent encore plus facilement étudier l’action d’un gène. De plus cette méthode peut être utilisée en parallèle sur différents gènes d’une même cellule permettant ainsi de faciliter l’étude des interactions entre les gènes. La méthode CRISP-Cas9 peut être utilisée sur des cellules in vitro mais aussi des œufs fertilisés (le stade unicellulaire de l’embryon). Enfin des recherches essayent d’améliorer cette technique encore jeune, ainsi à la place de la protéine Cas9, il est possible d’utiliser la protéine Cpf1 plus efficace pour l’insertion d’ADN. Au-delà des laboratoires, cette technique intéresse tous les acteurs des biotechnologies.
Éthique
Mais cette nouvelle technique rend encore plus prenante les questions d’éthique autour de l’édition de génome. Une des principales questions est l’utilisation chez l’humain et, en particuliers, chez l’embryon avec des questions d’eugénisme possible. Une étude publiée fait déjà cas de la modification d’embryon humain qui n’étaient pas viables. Si les chercheurs du monde entier semblent d’accord pour ne pas poursuivre ces recherches, rien ne le garantie et la diversité des réglementations dans les différents pays ne garantit pas que cela ne se fera jamais. D’autant que des embryons viables ont été obtenus dans des espèces proches comme des singes, des chiens… Pour l’instant, c’est chez le cochon que le plus de modifications sont faites dans l’optique d’obtenir des animaux donneurs d’organes le plus proche possible des humains.
L’autre question d’éthique est le couplage des méthodes CRISPR a un « gene drive ». Lors de la modification du génome d’un embryon, il est possible d’insérer en plus du gène modifié, le gène de Cas9 (ou Cpf1) et la séquence ADN codant pour le ARN guide de Cas9. Cette modification modifiera d’elle-même le gène sur le l’autre chromosome. Ainsi l’individu créé est porteur uniquement de la version modifié du gène et tous ses descendants également. Ils hériteront d’un chromosome modifié qui modifiera le chromosome venant de l’autre parent. De cette façon, le gène modifié se répandra rapidement dans la population. La première application envisagée est chez Anophèle vecteur du paludisme pour les rendre résistant au parasite et éliminer la maladie. Ce type de modifications semble très prometteur mais pause d’énorme question sur l’effet sur les populations sauvages et l’équilibre des écosystèmes. De plus, mais si cette méthode est utilisée dans une population isolée et précise dans une volonté de conservation ou de restitution d’un écosystème, il est impossible d’être sûr qu’un individu modifiés ne se retrouve pas dans une autre population ou de se croiser avec une espèce proche.
Pour cette quatrième saison, Orphan Black propose toujours une très bonne science-fiction, qui n’est jamais très loin de la réalité sans l’être pour autant. Elle propose une intrigue toujours prenante et se resserrant sur la néolution. Elle arrive toujours à surprendre le spectateur et propose des alliances des plus improbable mais compréhensible aux vues des événements. Elle manie très bien l’équilibre entre une histoire très sombre et de l’humour au détour des différentes situations. Enfin si la saison présente moins de clones que certaines, elle continue à bien développer ceux qui sont là et tous ont leur moment de mise en avant. BBC America a annoncé que la prochaine saison (cinquième) serait également la dernière. Ce qui est pour moi une plutôt bonne nouvelle, cela nous assure une histoire finie, satisfaisante et sans perte de qualité. Cela se sont aussi dans cette saison (surtout sa fin) où les différents éléments se mettent en place et où nos chères clones semblent enfin avancer.
Pas tout compris ? Tu as des remarques ? Une erreur s’est glissée dans le texte ? N’hésite pas à laisser un commentaire, j’y répondrais avec plaisir.
Pour aller plus loin :
La vidéo de Science étonnante Modifier le génome avec CRISPR/Cas9
Les articles de CNRS Le journal sur l’édition du génome
L’article de Nature qui fait le point sur CRISPR (en anglais mais les illustrations sont intéressantes)
La vidéo de Kurzgesagt – In a Nutshell Genetic Engineering Will Change Everything Forever – CRISPR en anglais avec des sous-titres français
L’article Pearls de PLOS Pathogens sur les défenses des bactéries contre les virus (en anglais et pointu)
Note perso :
[star rating= »5″]
Orphan Black, 2013 (en production)
Créée par Graeme Manson, John Fawcett
Avec Tatiana Maslany, Dylan Bruce, Jordan Gavaris plus
Nationalité Américaine, canadienne (BBC America)
Format 42 minutes
La bande annonce en VO (non sous-titrée):
